MONSERRAT RIPOLL C., CARDONA PERETO J., LLÁCER BORRÁS F., ORTEGA ANDRÉS C., TARÍN-ROYO, F. RAMOS BODI C.
Introducción
Desde que en 1.933 se implantara el primer marcapasos externo, seguido en 1.958 del primer implante de marcapasos definitivo, millones de pacientes se han beneficiado de este dispositivo con el fin de aumentar supervivencia, mejorar calidad de vida y tratar arritmias cardiacas que, sin este dispositivo, hubieran sido incompatibles con la vida.
En el año 2.009 se implantaron en España 34.103 marcapasos, y más de 400.000 en el mundo 1.
Se ha producido un cambio significativo no sólo en los generadores y electrodos, sino también en las indicaciones de estimulación, modos de estimulación y seguimiento a través de telemetría. Actualmente, la tecnología ha puesto a disposición de la ciencia médica grandes avances de ingeniería, aportando nuevos marcapasos fisiológicos que respetan la sincronía auriculoventricular lo que ha permitido mejorar la calidad de la vida, además de la supervivencia, minimizar las complicaciones postimplante y optimizar el tratamiento de las bradiarritmias.
Componentes de los Marcapasos
Podemos diferenciar 4 componentes en un marcapasos:
1.- Fuente de energía o Generador: Se encarga de suministrar el impulso eléctrico a través de los electrodos al corazón. Las más utilizadas actualmente son de yodo-litio. Generalmente, está formado por un electrodo positivo (ánodo) o un electrodo negativo (cátodo), separados por un medio electrolítico de conducción iónica.
2.- Circuito Electrónico: La energía que aporta el generador debe ser modificada por un circuito de programación para que el impulso salga con una frecuencia, amplitud y duración determinada. La frecuencia del marcapasos viene determinada por un oscilador de cristal asociado a un circuito de sensado que permite la detección de la actividad cardiaca intrínseca a través del sistema de electrodos, dando lugar a los sistemas de estimulación de demanda y secuenciales.
3.- Carcasa (figura 1): Fabricado por material biocompatible, contiene el cabezal de las conexiones que presenta de 1 a 3 entradas para cada uno de los conectores que se suelen fijar con uno o dos tornillos. Es la parte externa del marcapasos, su misión es contener los componentes del circuito del generador. Debe dar soporte mecánico, proteger de la humedad y servir de aislante.
Figura 1. Carcasa de marcapasos
4.- Electrodos (figura 2 y 3): Es la parte del sistema de estimulación cardiaca que trasmite el impulso eléctrico desde el generador hasta el miocardio. El material del electrodo debe ser conductor, debe estar aislado y su calibre debe ser adecuado para introducirse por el sistema venoso.
Los electrodos pueden ser unipolares o bipolares, los primeros son cables que sólo tienen un polo de estimulación situado en el extremo distal en contacto con el miocardio, siendo el polo positivo la propia carcasa del marcapasos; esto hace que este sistema sea más susceptible a interferencias externas, ya que puede detectar miopotenciales que lleven a la inhibición del marcapasos. Por este motivo, actualmente son más utilizados los electrodos bipolares, estos están constituidos por dos polos para estimulación y detección, uno situado en el extremo distal, el negativo y el polo positivo situado aproximadamente a 3 cm del primero. Una clara ventaja del electrodo bipolar frente al unipolar es el menor riesgo a captar interferencias.
Figura 2.
Muchos generadores incluyen la polaridad como un parámetro programable, siendo posible programar la estimulación unipolar, que permite mejor visualización de las espículas en un ECG de superficie y la detección bipolar para disminuir el riesgo de interferencias.
Del mismo modo los electrodos pueden ser de fijación activa o pasiva, según el modo de fijación al endocardio.
Figura 3.
Indicaciones de Implante de Marcapasos
Las indicaciones de implantar un marcapasos según las principales patologías han sido dispuestas por el Colegio Americano de Cardiólogos (ACC) y la Asociación Americana del Corazón (AHA), que forman grupos de práctica clínica en las que se especifican las normas de actuación según la evidencia recogida de las publicaciones médicas y la experiencia personal de los cardiólogos implicados 2.
La Sociedad Española de Cardiología (SEC) ha desarrollado unas guías propias adaptando las del Journal of the American Collage of Cardiology (JACC) con las indicaciones para implantar un marcapasos según las principales patologías 3, que incluyen:
- Enfermedad del Nodo Sinusal (ENS).
- Bloqueo Auriculo-Ventricular adquirido en el adulto (BAV).
- Bloqueo bifascicular crónico.
- Hipersensibilidad del seno carotídeo y síndromes neuromediados.
- Post-fase aguda de Infarto de Miocardio.
- Estimulación cardiaca permanente en niños, adolescentes y cardiopatías congénitas.
- Indicaciones de marcapasos en la Miocardiopatía Hipertrófica.
- Indicaciones de marcapasos en miocardiopatía dilatada.
- Indicaciones de estimulación cardíaca tras el Trasplante Cardíaco.
- Antitaquicardia.
- Prevención taquicardia.
Tipos y Modos de Marcapasos
Tipos
Los marcapasos pueden ser Temporales o Permanentes, dependiendo de si la causa que obliga al implante del marcapasos es o no reversible.
- Temporales: Las principales indicaciones de implante de marcapas temporal son bradicardia con compromiso hemodinámico, BAV completo, complicación de infarto agudo de miocardio con trastornos en la conducción, BAV o bloqueo de rama de reciente aparición en la endocarditis sobre válvula aórtica, sobredosis de fármacos. Pueden ser:
· Transcutáneos: utilizados en caso de extrema urgencia con los electrodos situados en el tórax.
· Intravenosos: los electrodos llegan hasta el ventrículo derecho tras atravesar el sistema venoso generalmente por una vena de gran calibre (femoral, yugular…). En estos casos el generador no se implanta en el paciente.
· Transtorácico: Los electrodos se sitúan en las paredes epicárdicas de la aurícula o ventrículo
- Permanentes:
· Endocárdicos.
· Epicárdicos: generalmente utilizados en niños, con el fin de que el crecimiento no interfiera en la longitud de los electrodos. En estos casos el generador se suele implantar en la pared abdominal.
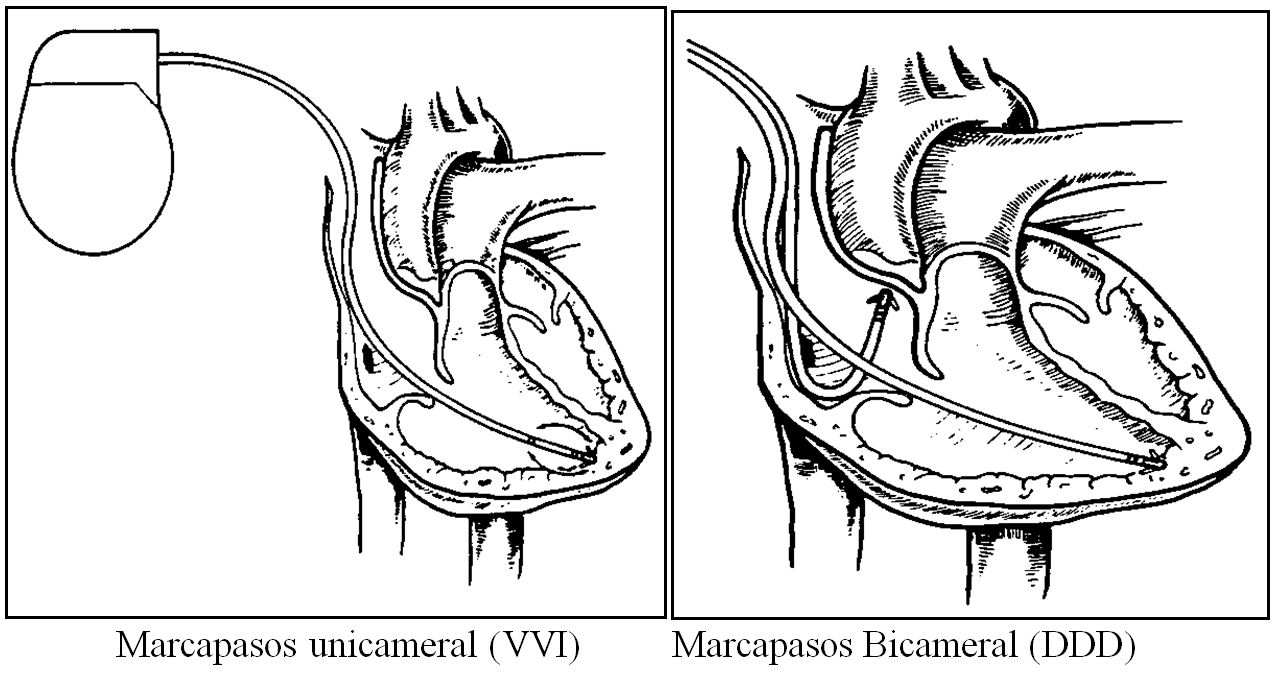
Dependiendo de los electrodos empleados, los marcapasos se pueden clasificar en uni o bicamerales (figura 4). Los primeros son aquellos en los que únicamente se estimula una de las cavidades cardiacas (aurícula o ventrículo).
Figura 4.
Los marcapasos bicamerales pueden emplear una o dos sondas; en el caso de emplear una sonda, ésta debe incorporar un electrodo de detección flotante que debe ser posicionado en aurícula derecha. En estos casos aumenta el riesgo de fallos en la detección auricular, ya que depende de la distancia del electrodo a la pared que se modifica con la contracción auricular y los cambios posturales.
Modos más frecuentes
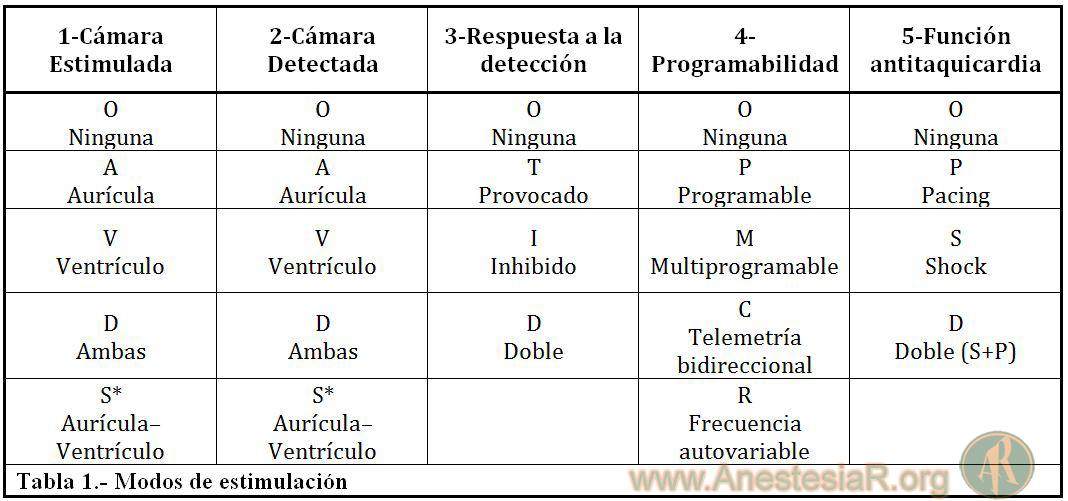
Para conocer los modos de estimulación más frecuente es imprescindible conocer el sistema de códigos revisado por la North American Society of Pacing and Electrophisiology/British Pacing Group (NASPE/BCG) 4, como se registra en la tabla 1:
La primera letra indica la cámara estimulada, pudiendo ser aurícula (A), ventrículo (V) o D (dual) si son ambas.
La segunda letra describe donde se produce la detección de la actividad intrínseca del corazón, pudiendo ser A para auricular, V para ventricular, D dual ambas cámaras u O si no hay sensado.
En las posiciones 1 y 2 se añadió la letra S como significado de Unicameral, para decir que el generador puede usarse tanto en aurícula como en ventricular.
La tercera letra indica el modo de acción del generador tras detectar la actividad cardiaca. La respuesta al sensado puede ser inhibición (I), disparo o triggered (T), ambas (D) o ninguna (O).
La cuarta letra indica las funciones programables. La presencia de la letra R en esta posición indica que el marcapasos contiene un sensor que puede modular la frecuencia de estimulación en función de la actividad física del paciente.
Por último, la quinta letra indica si el generador tiene funciones antitaquicardia. Actualmente estas funciones se han incorporado a los desfibriladores automáticos implantables (DAI) para el tratamiento de las taquicardias ventriculares.
Conociendo estos símbolos podemos deducir los modos de estimulación más frecuentes:
- VVI: estimula y detecta solo en ventrículo.
- AAI: estimula y detecta sólo en aurícula.
- VDD: estimula en ventrículo y detecta en ambas cámaras.
- DDD: estimula y detecta ambas cámaras.
Cómo seleccionar el modo de función del marcapasos
Como ya hemos dicho, la estimulación cardíaca puede ser unicameral (en aurícula o ventrículo) o bicameral.
- La estimulación auricular obtiene el mejor resultado hemodinámico, ya que permite la conservación del sincronismo AV, pero si existe alteración de la función sinusal con imposibilidad de taquicardización al esfuerzo, su resultado sobre el aumento del gasto cardíaco es muy limitado. La incorporación de un biodetector con posibilidad de modular las frecuencias de estimulación puede ser de ayuda en estos casos.
1.- Los biodetectores 5 más utilizados en la práctica clínica son los que responden a la actividad. Este mecanismo piezoeléctrico está situado en su interior y detecta fuerzas mecánicas o vibraciones (movimiento del cuerpo), que son transformadas en energía eléctrica para el control de la frecuencia cardíaca. Este biodetector no es metabólico y, por tanto, no es fisiológico: no responde al ejercicio mental, a las emociones o al ejercicio isométrico. Es un sistema simple, fiable, estable, fácil de programar, usa un electrodo estándar y tiene una respuesta rápida a períodos breves de ejercicio.
2.- Los marcapasos dependientes de la respiración son dispositivos que calculan el volumen ventilatorio por minuto a partir de la impedancia transtorácica 6, asumiendo que el volumen por minuto respiratorio calculado se correlaciona estrechamente con las demandas metabólicas.
3.- Existen otros tipos de biodetectores menos utilizados en la práctica clínica, como las basados en cambios de la temperatura o del intervalo QT, y en la actualidad se están investigando biodetectores que detectan cambios en la aceleración endocárdica.
4.- Últimamente ha aparecido una nueva generación de marcapasos que utilizan dos biodetectores para utilizar las ventajas de cada uno de ellos y evitar sus inconvenientes (existen varias posible combinaciones: por ejemplo, actividad e intervalo QT, actividad y frecuencia respiratoria, actividad y aceleración endocárdica, etc.) 7.
El gran problema no resuelto de los marcapasos de frecuencia adaptable es cómo programar sus parámetros ante un paciente determinado. En general, se ha descrito que la programación adecuada debería ser la que incrementase la frecuencia cardíaca de 10 a 25 lat/min. (hasta 90 por min.), ante un paseo de 2 ó 3 min., o que en un paseo rápido o subir escaleras aumentase la frecuencia de 20 a 45 lat/min. (hasta 100 a 120 por min.) 8.
- En los pacientes con bloqueo AV y función sinusal normal, la estimulación secuencial es el modo que consigue el mayor beneficio hemodinámico, por lo que en estos casos está indicado el marcapasos bicameral con uno o dos electrodos 9. Es el caso del Marcapasos VDD con electrodo único, indicado en los pacientes con bloqueo AV de segundo o tercer grado que tienen preservada la función sinusal y no es necesaria la estimulación auricular, y la estimulación ventricular atriosincrónica es la ideal.
La estimulación VDD con electrodo único está contraindicada en:
· Enfermedad del nódulo sinusal.
· Fibrilación o flúter auricular crónico.
· Cardiomegalia significativa (dilatación de aurícula derecha).
· Imposibilidad de detectar potenciales endocavitarios auriculares adecuados durante la implantación.
En la tabla 2 se expone la selección del modo de estimulación tras valorar el estado de la función sinusal, el cronotropismo y la conducción auriculoventricular. Al seleccionar el modo de estimulación adecuado para el paciente se deben tener en cuenta una serie de factores que inclinarán hacia uno u otro modo. Dichos factores son la edad, estado general y existencia de enfermedad asociada (cardíaca o no), tipo de trastorno del sistema excitoconducción que condiciona la implantación, género de vida del paciente y su capacidad funcional 10.
Técnica de Implante de Marcapasos
Idealmente el implante del marcapasos debe llevarse a cabo en un quirófano. En su defecto, puede realizarse en una sala de hemodinámica o de radiología, siempre con estrictas condiciones de asepsia.
Recursos materiales
Los requerimientos básicos para este lugar serían:
- Disponer de oxígeno, toma de vacío, aspiración, gases anestésicos, aislamiento eléctrico, aislamiento radiológico y luz quirúrgica.
- Sistema de fluoroscopia con intensificador de imagen y mesa radiotransparente.
- Material quirúrgico adecuado, y duplicado en cada procedimiento, para poder atender a su sustitución completa en caso de contaminaciones: campos estériles, bisturí, mosquitos, pinzas, tijeras, portas, suturas, electrocoagulador.
- Material para acceso y mantenimiento de vías intravenosas.
- Monitorización continua electrocardiográfica y pulsioximetría.
- Sistema analizador de umbrales de marcapasos.
- Programador del marcapasos que se implante.
- Desfibrilador-cardioversor y marcapasos externo transcutáneo.
- Material de emergencia que debe incluir todo lo necesario para una resucitación cardiopulmonar avanzada, para la realización de pericardiocentesis y drenaje torácico.
Técnica
El implante del marcapasos se puede realizar bajo anestesia local y sedación.
El paciente se debe colocar en decúbito supino. Se canaliza, tras esterilización de la zona, la vena subclavia o se realiza la disección de la vena cefálica. A la hora del implante se elegirá el lado opuesto a la mano dominante del paciente para disminuir la posibilidad de aparición de interferencia por miopotenciales y para evitar la activación incorrecta de biosensores sensibles a la actividad física.
Mediante la técnica de Seldinger se introducen los electrodos hasta su correcto posicionamiento guiado por fluoroscopia. Cuando las puntas de los electrodos están bien situadas se miden los umbrales con el analizador de umbrales y si los datos son correctos se procede a la fijación de los electrodos y al implante del generador.
Conceptos básicos para el implante y el seguimiento del marcapasos
Para asegurar la correcta posición de los electrodos es fundamental medir los parámetros eléctricos que corroboran la correcta colocación de los mismos. Estos parámetros se basan en el contacto entre el electrodo y el miocardio 11.
- Amplitud de la señal intracardiaca (mV): Esta medida indica la calidad del contacto del electrodo, así como la comprobación de la colocación del electrodo en la cavidad correcta. Los electrodos son responsables de enviar al dispositivo la señal intracardiaca asociada a la actividad intrínseca del corazón, es decir la contracción miocárdica, con el fin de que el generador interprete dicha señal como propia y se inhiba su funcionamiento en caso de que haya estímulo. El nivel de señal que es capaz de interpretar el dispositivo se conoce también como sensibilidad. Clásicamente, se aceptan medidas de ondas R > 5 mV para ventrículo y ondas P > 2 mV para aurícula.
- Impedancia (Oh): La medida de la impedancia asegura un buen contacto. Sirve tanto en el implante como en las siguiente revisiones para comprobar la integridad de los electrodos. Una caída de la impedancia reflejaría una rotura del aislamiento que provocaría alteraciones en la detección. Por el contrario, un aumento de la impedancia nos haría sospechar rotura del conductor, dislocación del electrodo o algún problema en la conexión. En el seguimiento de los marcapasos es fundamental conocer la impedancia de mediciones anteriores para poder conocer el estado del electrodo, ya que cambios de impedancia mayores a 200 Oh, podrían significar alteraciones en el electrodo y no debería demorarse la comprobación del correcto estado del electrodo, a pesar de que el paciente esté asintomático.
- Umbral de estimulación (V): Es el umbral conocido para la despolarización del miocardio al aplicar una corriente eléctrica sobre el miocardio, equiparable al umbral de despolarización de las células excitables, conocido como potencial de acción. La cantidad de energía mínima que se necesita para que dicho impulso eléctrico se siga de una respuesta de contractilidad del miocardio es el Umbral de Estimulación. Es importante conseguir durante el implante un umbral de estimulación con la menor amplitud de impulso posible. Se considera como un buen umbral de estimulación durante el implante aquel umbral inferior a 1 V, consiguiéndose gracias a los avances tecnológicos umbrales de 0,4-0,6 V.
Por norma general, tras el implante del marcapasos se realiza un ECG de superficie y una Radiografía de Tórax.
Complicaciones
Las complicaciones tras el implante del marcapasos dependen de la técnica empleada, de la habilidad del implantador y del tipo del marcapasos (suelen ocurrir más complicaciones en los marcapasos bicamerales).
Por otra parte, las complicaciones pueden ser precoces, aquellas que ocurren en el primer mes tras el implante o tardías, las que se producen después del primer mes. Lógicamente, las complicaciones precoces suelen ir ligadas a la técnica de implante y pueden ser:
- Punción accidental de arteria, nervio, conducto torácico, pleura.
- Arritmias.
- Perforación cardiaca con riesgo de taponamiento cardiaco, estimulación del ventrículo izquierdo o estimulación extracardíacas (diafragmática).
- Rotura accidental del electrodo o mala conexión.
- Síndrome de la vena cava superior.
- Trombosis venosa.
Como complicaciones en relación con el bolsillo que aloja el generador se pueden presentar:
- Hematoma.
- Dehiscencia de la sutura de la pared.
- Migración del marcapasos.
- Erosión.
- Protusión.
- Dolor.
- Infección del bolsillo.
- Alergia al marcapasos.
Interferencias sobre el Marcapasos
Se definen las interferencias electromagnéticas como las señales eléctricas de origen no fisiológico que afectan, o pueden afectar, a la función normal de un marcapasos 12. Los marcapasos definitivos como detectores de señales eléctricas, están sujetos a interferencias desde fuentes electromagnéticas.
Los sistemas de detección unipolar son más susceptibles de interferencias que los bipolares, ya que en aquellos programados con detección unipolar pueden sufrir interferencia a lo largo del electrodo, en cambio en la detección bipolar la longitud del electrodo sobre el que se pueden producir interferencias es muy pequeña.
Los marcapasos bicamerales son más susceptibles de sufrir interferencias que los monocamerales debido a que poseen dos electrodos sobre los que se puede producir interferencia.
El uso de electrodos bipolares y los avances tecnológicos en los generadores han disminuido el riesgo de interferencias.
Las principales fuentes de interferencia, en el área médica, que afectan a los MP son: Electrocoagulador, Desfibriladores, Resonancia Magnética, Litotricia y Estimulación nerviosa transcutánea 13.
- Electrocoagulador, electrocauterio o bisturí eléctrico:
Los posibles efectos sobre el marcapasos al utilizar un bisturí eléctrico son:
· Inhibición de uno o varios latidos o total: La interferencia puede ser interpretada como un impulso cardiaco provocando inhibición inapropiada del marcapasos, o como un ruido provocando un cambio de modo a VOO con la consiguiente asincronía auriculo-ventricular y trastorno hemodinámico.
· Fallo permanente en la función del marcapasos por daño sobre la circuitería.
· Daño miocárdico por conducir el electrodo, señales producidas por el electrocauterio, pudiendo causar quemaduras con posibilidad de aumento del umbral.
· Respuestas inesperadas en marcapasos con función reguladora de frecuencia.
· Anulación de función en algunos casos con signos de depleción de la batería.
Como recomienda la ASA y su “Task Force on Perioperative Management of Patients with Cardiac Rythm Management Devices” 14, en la evaluación preoperatoria se debe:
· Realizar una anamnesis detallada del enfermo, buscar revisiones médicas anteriores, Rx de tórax y ECG.
· Examen físico del paciente buscando cicatrices y palpar el dispositivo.
· Averiguar el tipo de dispositivo.
· Comprobar la dependencia del enfermo con el MP: si tiene ritmo propio o no, para ello es útil conocer la causa del implante, los síntomas previos.
· Evaluar el modo de funcionamiento y el estado del dispositivo, Es aconsejable desactivar la función “R” de autofrecuencia y los algoritmos no imprescindibles para la estimulación.
Durante la intervención:
· No se debe usar el electrobisturí a una distancia menor de 15 cm de la zona del marcapasos o punta de electrodo, y nunca entre ambos. En pacientes sujetos a reemplazo del generador y con signos evidentes de depleción de la batería también debería evitarse su uso.
· Se debe usar el cauterio bipolar siempre que sea posible. No utilizar el cauterio cerca del marcapasos, y cuando se utilice en general con toques cortos y repetidos.
· Monitorizar, a parte del ECG, la pulsioximetria que nos ayudará a discriminar la presencia o no de pulso.
· Usar el IMAN sobre el dispositivo durante la utilización del cauterio, hace que el MP se ponga en modo VOO a la frecuencia magnética, es decir, sin poder ser influenciado por estímulos externos a una frecuencia fija determinada por el marcapasos, al retirar el imán el MP vuelve a funcionar en el modo en que estuviera programado con anterioridad.
En el postoperatorio se debe comprobar el normal funcionamiento del dispositivo.
- Desfibrilación y Cardioversión:
La desfibrilación eléctrica externa conlleva una gran cantidad de energía que es trasmitida al miocardio y en pacientes portadores de marcapasos, dada su proximidad a éste, se pueden ocasionar daños tanto en el generador como en el miocardio produciéndose una quemadura miocárdica en el punto de contacto con el electrodo distal.
Los posibles efectos que se puede presentar tras una cardioversión son el cambio de modo, aumento de umbral e infradetección.
El grado del daño miocárdico parece relacionarse con la distancia de las palas al generador, por ello todos los fabricantes recomiendan colocar las palas lo más lejos posible del marcapasos.
Recomendaciones para pacientes que van a ser sometidos a Desfibrilación/Cardioversión:
· Antes del procedimiento:
* El programador del MP debe estar a mano para reprogramar y evaluar.
* Determinar el grado de dependencia si es posible antes de la cardioversión.
* Tener disponible un MP externo transtorácico.
* Usar la menor cantidad de energía posible.
* Nunca aplicar las palas sobre el marcapasos.
· Después del procedimiento:
* Repetir test de sensado y umbral tras la desfibrilación.
* Monitorizar al menos 12 horas.
- Resonancia Magnética (RMN):
Utiliza un gran campo magnético generado por un electro imán y formado por ondas de alta frecuencia. Los marcapasos más antiguos, pueden experimentar una fuerte presión en la zona donde se aloja el generador.
Los problemas publicados más recientemente han sido la activación asincrónica del MP, inhibición inapropiada, frecuencias rápidas, cambio de modo de DDD a VVI o VOO y malfunciones transitorias.
Las recomendaciones generales apuntan a que los pacientes con MP no se sometan a RMN, excepto en casos estrictamente necesarios. En ese caso, los marcapasos deben programarse en VOO si el paciente es MP dependiente y utilizar la opción imán “off” en aquellos marcapasos que esté disponible. Y en pacientes no dependientes de marcapasos utilizar la opción de desconexión del generador si se dispone de ella. Se debe emplear una bolsa de hielo frío sobre el dispositivo. Una vez terminado el procedimiento se debe realizar un chequeo del dispositivo.
Recientemente han salido al mercado, los primeros dispositivos que permiten la realización de RMN minimizando el riesgo de interferencias, así como electrodos útiles también para el mismo caso.
- Litotricia:
Se sabe que cuando las ondas de choque son síncronas el MP no sufre inhibición, en cambio cuando son asíncronas se producen inhibiciones tanto en los marcapasos programados como unipolares como en los bipolares. Este riesgo es menor en las unidades unicamerales que en las bicamerales. Se han registrado también alteraciones en la frecuencia en los marcapasos con “R”, quizá este sea el mayor inconveniente.
En general sólo se han detectado daños físicos en el MP cuando las ondas se han dirigido directamente hacia ellos (generadores situados en el abdomen). Se aconseja desactivar la “R” mientras se realiza el procedimiento.
- Estimulación eléctrica transcutánea (TENS):
Puede causar inhibición en los marcapasos programados como unipolares ya que las ondas producidas se asemejan a la señal cardiaca. Esto puede evitarse disminuyendo la sensibilidad del dispositivo. En los portadores de VDD y DDD puede ocasionar aumento de frecuencia cardiaca por sensados inadecuados de la aurícula y conducción al ventrículo. Pueden usarse con seguridad en pacientes con dispositivos bipolares
- Equipo dental:
El uso de equipos para realizar técnicas dentales pueden interferir con los marcapasos por el uso del fresado y los ultrasonidos, aunque ninguna de ellas es capaz de deteriorar los dispositivos. Es más frecuente en dispositivos con biodetector de actividad que son capaces de detectar las vibraciones del fresado.
Se recomienda para disminuir el riesgo de interferencias:
· Utilización intermitente del procedimiento de fresado o de ultrasonidos.
· No apoyar los instrumentos sobre el generador.
· Desprogramar la modulación de frecuencias durante las sesiones.
- Radiación:
En casos de radioterapia se puede producir una desprogramación del dispositivo, provocando anomalías en la detección y en la estimulación.
Como norma general, se recomienda:
· Evitar la irradiación terapéutica sobre el generador (si no es posible se ubicará el marcapasos en el otro hemitórax).
· Proteger el generador durante las sesiones de radioterapia.
· Análisis del generador tras cada una de las sesiones.
- Electroshock:
Durante esta técnica sólo una pequeña cantidad de electricidad alcanza al corazón debido a la alta resistencia de los tejidos corporales.
· No se daña el marcapasos
· Se crean miopotenciales capaces de inhibir el marcapasos con detección monopolar.
Se aconseja la monitorización del ECG durante la técnica y posteriormente análisis del generador.
Bibliografía
1.- Coma R. Registro Nacional de Marcapasos BNDM 2009 (web)
2.- Gregoratus G, Cheitlin MD, Conill A et al. ACC/AHA guidelines for implantation of cardiac pacemakers and antiarrhytmia devices: a report of the American College of Cardiology/American Heart Association Task Force on practice guidelines (Committee on Pacemaker Implantation). J Am Coll Cardiol 1998; 31: 1175-1209. (PubMed)
3.- Oter R, De Juan J, Roldán P, Bajardí A, Molinero E. Guias de practica clinica de la Sociedad Española de Cardiología en marcapasos. Rev Esp Cardiol. 2000; 58(12):947-966. (PubMed) (pdf)
4.- Bernstein AD, Camm J, Fletcher RD et al. The Naspe/BPEG generic pacemaker code for antibradyarrhythmia and adaptative-rate pacing and antitachyarrhythmia devices. PACE 1987; 10: 794-799. (PubMed)
5.- Bacharach DW, Hilden TS, Millerhagen JO, Westrum BL, Kelly JM. Activity-based pacing: comparison of a device using an accelerometer versus a peioelectric crustal. PACE 1992; 15: 188. (PubMed)
6.- Santomauro M, Fazio S, Ferraro S et al. Follow-up of a respiratory rate modulated pacemaker. PACE 1992; 15: 17-21. (PubMed)
7.- Cerezuela J.L. Funciones automáticas en los marcapasos implantables. En De Teresa E. Castro-Beiras A. Editores. Marcapasos. Manual para el cardiólogo clínico. 1999; 75-101. (googlebooks)
8.- Hayes DL, VonFeldt L, Higano ST. Standardized informal exercise testing for programming rate adaptative pacemakers. PACE 1991; 14: 1772-1776. (PubMed)
9.- Rey JL, Tribouilloy C, Elghelbazouri F, Otmani A. Single-lead VDD pacing: long-term experience with four different systems. Am Heart J 1998; 135: 1036-1039. (PubMed)
10.- Méndez- Rosabal A. Marcapasos. Indicación, seguimiento e implante. (pdf)
11.- Garcia-Urra F. Funciones programables. En: Garcia-Urra F, Porres-Aracama JM Editores. Práctica clínica en electrofisiología, Marcapasos definitivos y desfibrilador automático. 3ª edición 2009; 101-112. (googlebooks)
12.- De Juan J, Cay E, Madrid A et al. Las interferencias electromagnéticas en los pacientes portadores de marcapasos. Revista Aragonesa de Cardiología 1995; 1: 17-23. (pdf)
13.- Garcia-Urra F. Interacciones con los marcapasos definitivos. En: Garcia-Urra F, Porres-Aracama JM Editores. Práctica clínica en electrofisiología, Marcapasos definitivos y desfibrilador automático. 3ª edición 2009;217-227. (googlebooks)
14.- Zaidan JR, Atlee JL, Belott P et al. Practice Advisory for the Perioperative Management of Patients with Cardiac Rhythm Management Devices: Pacemakers and Implantable Cardioverter-Desfibrillators. Anesthesiology 2005; 103:186-198. (PubMed) (pdf)
Monserrat Ripoll C., Cardona Pereto J., Llácer Borrás F., Ortega Andrés C., Tarín-Royo, F. Ramos Bodi C.Hospital de Dénia, Alicante.