 RAQUEL LÓPEZ LÓPEZ
RAQUEL LÓPEZ LÓPEZ
Referencia Completa: Erden V, Erkalp K, Yangin Z, Delatioglu H, Kiroglu S, Ortaküz S, Ozdemir B. The effect of labor on sevoflurane requirements during caesarean delivery. Int J Obstet Anaesth. 2011 Jan; 20(1): 17-21. (PubMed) (pdf)
Introducción
Como parte de la respuesta neuroendocrina al estrés el trabajo de parto desencadena la liberación de cortisol y otras sustancias tales como progesterona, prolactina, prostaglandinas y citokinas.
Se ha demostrado que algunas de estas sustancias parecen intervenir en la regulación del sueño o presentan efectos “benzodiacepin-like”.
Se plantea la hipótesis de que, en pacientes con trabajo de parto establecido que van a ser sometidas a cesárea bajo Anestesia General (AG), dichas sustancias puedan disminuir los requerimientos de Sevoflurano.
Resumen
Métodos
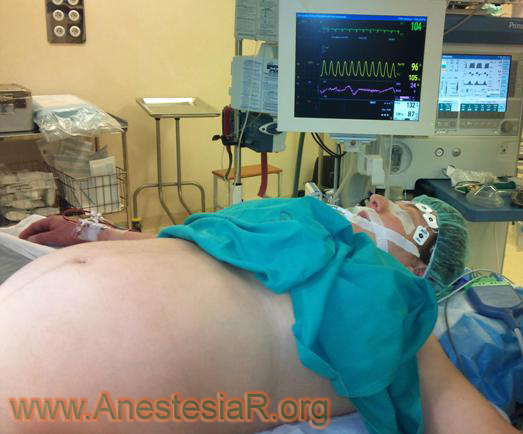
Tras aprobación por el Comité de Ética se obtiene consentimiento informado de 50 parturientas sanas que solicitan AG para cesárea.
Criterios de exclusión pacientes con: gestación gemelar, sufrimiento fetal preoperatorio, anormalidades fetales, preclampsia y enfermedades endocrinometabólicas.
Establecen 2 grupos de estudio, según los valores de la actividad uterina:
- Grupo Prelabor: n=25, ≥ 39 semanas de gestación, < 30 unidades Montevideo.
- Grupo Labor: n=25, 1er estadio de trabajo de parto en las 48 h previas sin analgesia, > 80 unidades Montevideo.
Miden niveles en sangre de Prolactina, Progesterona y Cortisol a todas las pacientes antes de la cirugía.
Monitorización estándar con ECG, PANI, temperatura, SatO2 y BIS, control de valores de basales y cada 2,5 minutos durante la intervención.
La inducción se realiza con tiopental 4-5 mg/kg, rocuronio 0,5mg/kg y tras IOT se mantiene la anestesia con 50% O2/N2O y Sevofluorano para conseguir valores de BIS entre 40-55 y ventilación mecánica adecuada para EtCO2 31-35 mmHg. Los valores de EtSev (%) y de EtCO2 (mmHg) son medidos cada 2,5 minutos desde la IOT
Tras la extracción fetal se administran 10 UI de Oxitocina y 1 µg/kg Fentanilo. Se revierte el bloqueo al final de la intervención con Atropina y Neostigmina y las pacientes son extubadas en quirófano.
Resultados
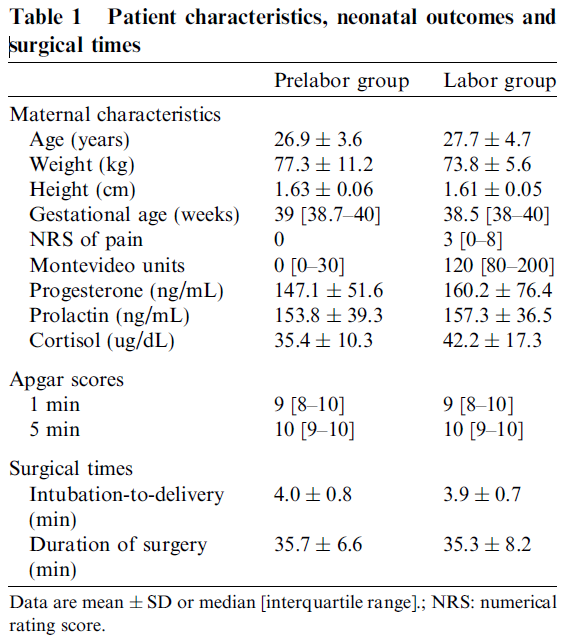
La tabla 1 resume los resultados obtenidos sobre las variables dependientes de las pacientes, puntuaciones neonatales y tiempos quirúrgicos. Reseñar que para todos ellos no se aprecian diferencias entre grupos.
Los niveles de Progesterona (p=0,48), Prolactina (p=0,75) y Cortisol (p=0,09) fueron similares.
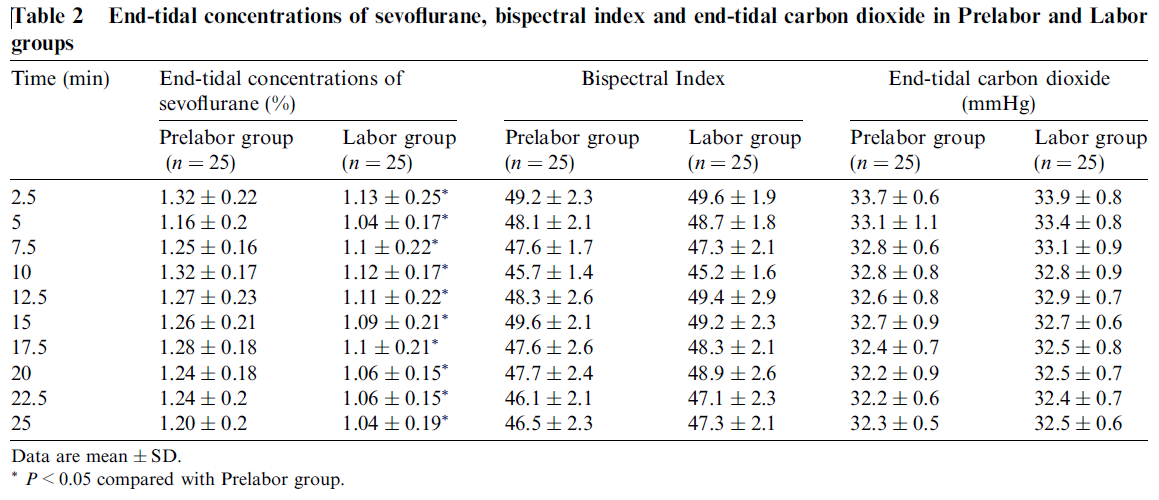
La tabla 2 muestra los valores de EtCO2, EtSev y BIS de los dos grupos.
Los valores de EtSev en el grupo Prelabor superan en todos los casos al grupo Labor (p< 0,05), sin que existan diferencias estadísticamente significativas en los valores del BIS ni del ETCO2.
Tampoco hubo diferencias en los valores de FC, PANI, SatO2 y temperatura.
Discusión
Estudios previos1 demuestran una menor necesidad de anestésicos inhalatorios en presencia de trabajo de parto establecido. El que analizamos es el único que valora la cantidad de inhalatorio necesaria para mantener valores estables de BIS y que además trata de encontrar el mecanismo causal.
Los autores demuestran que, en mujeres con trabajo de parto, las necesidades de Sevofluorano disminuyen, pero dicho efecto no parece ser debido a las diferencias en los niveles de Cortisol, Prolactina o Progesterona.
Como limitaciones al estudio se considera:
- Posible afectación de los niveles de BIS por factores demográficos (bien controlados en el estudio) o fisiológicos2.
- La variabilidad en los umbrales de actividad uterina para intensidad y frecuencia.
- Niveles de Cortisol limitados por el incremento de Cortisol unido a globulinas.
Ante la no demostración de la hipótesis causal, plantean la posibilidad del sistema opioide endógeno como responsable de los hallazgos.
Comentarios
Destacar el correcto tratamiento estadístico, con selección de tamaño muestral que prevé pérdidas y tratamiento diferenciado de variables paramétricas y no paramétricas.
Como aplicación de los resultados del estudio podemos disminuir la fracción inspirada del agente inhalado, manteniendo siempre valores estables de BIS, minimizando así el riesgo de despertar intraoperatorio2 (de mayor incidencia en la población obstétrica 0,4-1,3% vs 0,1-0,2%). También se disminuye el posible efecto tocolítico y riesgo hemorrágico, dosis dependiente, asociado a los inhalatorios.
Es interesante analizar el papel (no demostrado) de la Progesterona como mecanismo causal. Hormona de producción placentaria, encargada de la inactividad uterina y que sólo disminuye tras el alumbramiento. Tanto ella como sus metabolitos son potentes moduladores positivos del receptor tipo A del GABA3. Además de sus conocidos efectos depresores e hipnóticos, hay estudios4 que demuestran una disminución de los requerimientos anestésicos en mujeres, según la fase del ciclo menstrual y los niveles de progesterona asociados. Sin embargo, sus niveles no parecen estar elevados en el trabajo de parto.
En relación al sistema opioide endógeno reseñar que algunos estudios5 avalan el aumento de β endorfinas durante el trabajo de parto y antes de una cesárea. Sin embargo, otros plantean resultados contradictorios en relación a la tolerancia al dolor en las distintas fases de la gestación y del parto6. Serán necesarios más estudios que midan niveles de β endorfinas durante el proceso quirúrgico para corroborar esta hipótesis.
Recomiendo una lectura sobre el sistema opioide materno-fetal que, aunque un poco antiguo, me parece interesante7.
Por último, comentar que, aunque todas las cesáreas del estudio se realizan entre las 8-12 horas, para evitar la posible influencia de los ciclos circadianos, en el estudio no se valora el efecto que la falta de descanso y el agotamiento pueden tener en aquellas mujeres, que han podido estar hasta 48 horas con trabajo de parto y sin analgesia.
Bibliografía
1.- Yoo KY, Jeong CW, Kang MW et al. Bispectral index values during sevoflurane-nitrous oxide general anesthesia in women undergoing cesarean delivery: a comparison between women with and without prior labor. Anesth Analg 2008;106:1827–32. (PubMed) (pdf)
2.- Myles PS, Leslie K, McNeil J, Forbes A, Chan MT. Bispectral index monitoring to prevent awareness during anaesthesia: the B-Aware randomised controlled trial. Lancet 2004;363:1757–63. (PubMed)
3.- Paul SM, Purdy RH. Neuroactive steroids. FASEB J 1992;6:2311–22. (PubMed) (pdf)
4.- Erden V, Yangin Z, Erkalp K, Delatioglu H, Bahceci F, Seyhan A. Increased progesterone production during the luteal phase of menstruation may decrease anesthetic requirement. Anesth Analg 2005;101:1007–11. (PubMed) (pdf)
5.- Carvalho B, Angst MS, Fuller AJ, Lin E, Mathusamy AD, Riley ET. Experimental heat pain for detecting pregnancy-induced analgesia in humans. Anesth Analg 2006;103:1283–7. (PubMed) (pdf)
6.- Dunbar AH, Price DD, Newton RA. An assessment of pain responses to thermal stimuli during stages of pregnancy. Pain 1988;35:265–9. (PubMed) PMID 3226756
7.- Abboud TK. Maternal and fetal beta endorphin: effects of pregnancy and labour. Arch Dis Child. 1988 Jul;63(7 Spec No):707-9. (PubMed) (pdf)
Raquel López LópezHospital Universitario Virgen de la Arrixaca. Murcia.

No hay comentarios:
Publicar un comentario